


Il diabete di tipo 2, l’obesità e i disturbi metabolici correlati sono
cresciuti in modo significativo negli ultimi anni fino a costituire
uno dei problemi più gravi per la salute nelle nazioni industrializzate
e nei paesi in via di sviluppo. Questa ricerca illustra la possibilità
di un’innovazione nel campo della terapia antidiabetica e antiobesità.
Il diabete di tipo 2, che è presente nel
90% della popolazione diabetica
generale, viene spesso considerato una
conseguenza del benessere, in quanto
concorrono in modo decisivo alla sua
comparsa l'alimentazione eccessiva e
la sedentarietà. Nei paesi europei e
negli Stati Uniti la prevalenza è di
circa il 3%. I fattori genetici sono
molto importanti per la comparsa
della malattia e circa il 40% dei diabetici
di tipo 2 ha parenti di primo grado
(genitori, fratelli o figli) affetti dalla
stessa malattia. Molti studi documentano
una correlazione evidente tra l'incremento
del peso corporeo e l'aumentata
frequenza della malattia.
Anche la mancanza di attività fisica è
stata messa in relazione col diabete,
osservando come soggetti che lavorano
in campagna sono più esposti al
diabete quando si trasferiscono in città
dove svolgono attività più sedentarie e
tendono ad aumentare di peso. La
dieta è importante in quanto si è visto
che l'assunzione di cibi ad alto contenuto
calorico e di veloce digestione e
con poche fibre, determinano un
assorbimento più rapido ed incrementi
maggiori e più repentini della glicemia.
L’aggregazione nello stesso paziente di
alcuni disordini metabolici, ciascuno
dei quali è di per sé un noto fattore di
rischio cardiovascolare, ha fatto emergere
un nuovo stato patologico definito
“sindrome metabolica”, a cui sono
associate dislipidemia, ipertensione,
insulinoresistenza/intolleranza al glucosio/
iperglicemia e adiposità viscerale.
Dati recenti dimostrano che la prevalenza
di quest’alterazione metabolica
è davvero impressionante, visto che
si parla del 24% degli individui sopra
i 20 anni e del 30% sopra i 50 anni ed
è presente in circa il 90% dei pazienti
con diabete mellito di tipo 2.
Ad accompagnare la gravità della
patologia ci sono i costi sostenuti dal
Servizio Sanitario Nazionale. Secondo
uno studio farmacoeconomico, in
Italia all’inizio degli anni 2000 la spesa
diretta per ospedalizzazioni e cure
mediche di pazienti in sovrappeso,
obesi e affetti da malattie collegate era
circa di 23 miliardi di euro. Si stima
che negli ultimi dieci anni tale costo sia aumentato del 5%. Un terzo di
questi costi è assorbito dal diabete, che
ha una progressione allarmante (in
meno di 15 anni il costo è raddoppiato
e il numero dei diabetici e degli
obesi cresce continuamente).
Ma non sono solo i costi a preoccupare.
Del binomio diabete-obesità si
muore: un diabetico in sovrappeso ha
un rischio doppio di morte nell’arco
di 10 anni rispetto a un normopeso;
un obeso ha un rischio doppio rispetto
ad un sovrappeso.
La sfida per combattere questa “epidemia”
sarà, quindi, quella di aumentare
l'arsenale di innovativi strumenti diagnostici
e strategie di intervento per
prevenire e ridurre al minimo le complicanze
di queste patologie sulla
popolazione colpita. Nella prospettiva
terapeutica vi è una crescente necessità
di scoprire e caratterizzare meglio i bersagli
biologici specifici per progettare
futuri farmaci che siano più efficaci e
presentino minori effetti collaterali.
In questo contesto, i PPARs
(Peroxisome Proliferator-Activated
Receptors), che svolgono un ruolo cruciale
nella regolazione dell'omeostasi
metabolica, rappresentano certamente
un bersaglio biologico attraente per lo
sviluppo di nuovi farmaci. I PPARs sono
fattori di trascrizione facenti
parte della superfamiglia dei recettori
nucleari. Le conoscenze acquisite
hanno permesso di identificare gli isotipi
PPARα, PPARβ/δ e PPARγ, e
definirne la distribuzione. Sono stati
anche scoperti ligandi in grado di attivare
questi isotipi (Figura 1).
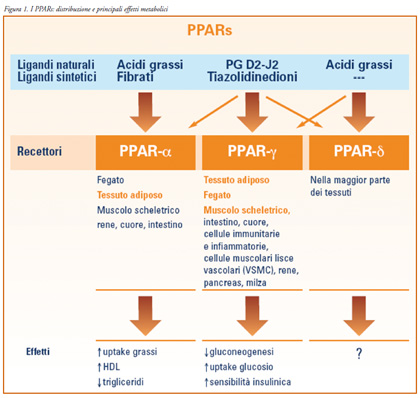
I PPARα agiscono fondamentalmente
sulla regolazione dell'omeostasi degli
acidi grassi e sembrano, quindi, essere
coinvolti nello sviluppo delle iperlipidemie.
L’esatto ruolo dei PPARβ/δ
non è ancora del tutto noto, ma si
pensa sia legato ai livelli di colesterolo
HDL.
I PPARγ sono stati trovati
soprattutto nelle cellule adipose, ma
anche in numerosi altri tessuti (epatici,
muscolari e cardiaci), sebbene in
quantità inferiori e recenti studi
hanno dimostrato che i PPARγ giocano
un ruolo importante nell’eziologia
del diabete tipo 2. Mutazioni geniche
del PPARγ sono infatti state correlate
con l’insulino-resistenza, benché non
sia ancora del tutto chiaro il meccanismo
che provoca una minor sensibilità
dell'organismo all’insulina e se le
mutazioni osservate siano causa diretta
o indiretta dei sintomi dell’insulino-
resistenza.
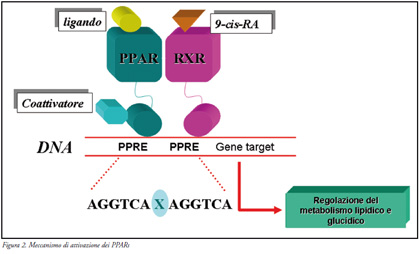
La Figura 2 mostra come i PPARs,
attivati da ligandi specifici, dimerizzano
con altri recettori nucleari, i recettori
per l’acido cis-retinoico (RXR).
Questo complesso binario, innescando
i meccanismi di rilascio di corepressori
e di ingresso di co-attivatori,
interagisce con specifici elementi
responsivi del DNA nucleare inducendo
l’espressione di proteine coinvolte
nei processi metabolici di proliferazione
e differenziazione adipocitaria,
lipogenesi, termogenesi, omeostasi glicemica
e sensibilità insulinica.
Sulla base di queste conoscenze, sono
stati sviluppati diversi farmaci che si
legano ai sottotipi α e γ come agenti
ipolipemizzanti (fibrati) e sensibilizzanti
dell'insulina (tiazolidinedioni)
rispettivamente, anche se recenti studi
clinici hanno sollevato dubbi sulla loro
sicurezza a causa degli effetti collaterali
connessi al loro utilizzo. Poiché gli agonisti
PPARα stimolano l'ossidazione
dei lipidi e promuovono la diminuzione
dell’adiposità e gli agonisti PPARγ
inducono un aumento di peso attraverso
gli effetti adipogenici, migliorando
l’insulino-resistenza, la combinazione
delle attività benefiche di entrambi
costituisce una prospettiva per il trattamento dell’obesità, del diabete e della
sindrome metabolica. Come è facilmente
intuibile, gli effetti biologici
dovuti all’attivazione di PPARα e
PPARγ sono tra loro opposti, quindi
la loro regolazione è molto fine ed il
prevalere dell’attività di uno su quella
dell’altro può dare luogo a gravi effetti
collaterali. Quest’ultimo aspetto è
quello che ha reso finora poco utilizzabili
i farmaci ipoglicemizzanti attivi su
PPAR-gamma ed i farmaci anti-lipidemizzanti
attivi su PPARα.
L’obiettivo delle nostre ricerche è stato
dunque quello di identificare attraverso
un approccio combinato computazionale,
sintetico, biologico e cristallografico,
nuovi composti con proprietà
di modulatori selettivi di PPARγ
(SPPARMs), cioè composti in grado
di attivare un set di geni target dei
PPAR solo in certi tessuti, minimizzando
così gli effetti collaterali.
I risultati
di questa ricerca, frutto di una
proficua collaborazione tra le Facoltà
di Farmacia dell’Università di Napoli
“Federico II”, Bari, Milano ed il CNR
di Roma, sono culminati nella scoperta
dell’ureido-fibrato LT127 che è un
agonista parziale dei PPARγ e si comporta
come uno SPPARM. Di particolare
rilievo è stato il lavoro da noi condotto per la messa a fuoco del
meccanismo molecolare che sta alla
base dell’agonismo parziale di LT127.
I risultati di questo studio sono stati
pubblicati sulla prestigiosa rivista
americana Journal of Biological
Chemistry.
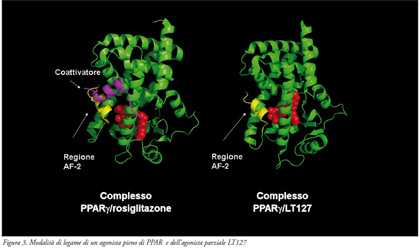
Tutti gli agonisti pieni di PPARγ,
come il rosiglitazone, condividono
una modalità di legame comune, che
coinvolge 3 residui aminoacidici
(Y473, H449 e H323) nel sito di legame
ed il gruppo acido del farmaco
(Figura 3).
Queste interazioni stabilizzano
la regione carbossi-terminale,
definita funzione di attivazione 2 (AF-
2), favorendo il legame del coattivatore
al recettore. Al contrario, LT127 si
lega al PPARγ in modo diverso.
Questa modalità di legame non coinvolge
direttamente la regione AF-2,
determinando così una ridotta capacità
di reclutare i coattivatori specifici
della differenziazione degli adipociti.
In conclusione, i risultati di questo
studio consistono nell’aver identificato,
attraverso un approccio multidisciplinare
(computazionale, sintetico,
biologico e cristallografico), LT127,
un composto capace di indurre solo la
trascrizione di uno specifico set di geni
target necessari per la sensibilizzazione
dei tessuti all’insulina, senza influenzare
i geni coinvolti nell’aumento della
massa grassa o promuovere altri effetti
collaterali.
Studi preliminari in vivo
mostrano che LT127 attiva geni target
di PPAR-gamma in modelli animali,
riduce i livelli di lipidi, glucosio ed
insulina nel sangue e riduce il peso
corporeo, principalmente attraverso
un’abbassamento della massa grassa.
In generale, LT127 mostra un profilo
farmacologico che influenza favorevolmente
lo stato metabolico di un
modello di topo obeso ed insulinoresistente,
rappresentando così il
primo passo verso lo sviluppo di farmaci
“intelligenti” per il trattamento
dell’obesità, del diabete e della sindrome
metabolica. La scoperta di LT127
come SPPARM offre pertanto, oggi,
la possibilità di un’innovazione nel
campo della terapia antidiabetica e
antiobesità, e apre la strada per l’ottenimento
di derivati con un profilo farmacologico
migliore, per i quali è prevedibile
un’ampia, rapida e competitiva
affermazione sul mercato internazionale.